
Rev Cuid. 2021; 12(2): e2025
http://dx.doi.org/10.15649/cuidarte.2025
RESEARCH ARTICLE
Diretrizes de prática clínica para o tratamento da Covid-19 no Brasil: uma revisão sistemática
Clinical practice guidelines for the treatment of
Covid-19 in Brazil: A systematic review
Guías de práctica clínica para el tratamiento de la enfermedad por Covid-19 en Brasil: revisión sistemática
Taís Carpes Lanes1, Mariane Albuquerque Lima Ribeiro2, Daianny Seoni de Oliveira3, Marcos Gabriel do Nascimento Junior4, Filipe Reis Garcia5, Jéssyca Maria França de Oliveira Melo6, Gustavo Magno Baldin Tiguman7
Recebido: 8 de dezembro de 2020
Aceito: 16 de abril de 2021
Publicado: 26 de julho de 2021
Como citar este artigo: Lanes, Taís Carpes; Ribeiro, Mariane Albuquerque Lima; Oliveira, Daianny Seoni de; Junior, Marcos Gabriel do Nascimento; Garcia, Filipe Reis; Melo, Jéssyca Maria França de Oliveira; Tiguman, Gustavo Magno Baldin. Diretrizes de prática clínica para o tratamento da Covid-19 no Brasil: uma revisão sistemática.Revista Cuidarte. 2021;12(2):e2025 http://dx.doi.org/10.15649/cuidarte.2025
![]() Atribución 4.0 Internacional (CC BY 4.0)
Atribución 4.0 Internacional (CC BY 4.0)
Resumo
Introdução: A Coronavirus Disease-2019 é uma doença infectocontagiosa que afeta o sistema respiratório, que surgiu na China e logo se espalhou pelo mundo. Objetivo: Avaliar a qualidade metodológica e transparência das Diretrizes de Prática Clínica brasileiras para o tratamento da Coronavirus Disease-2019. Materiais e Métodos: Trata-se de uma revisão sistemática realizada em 2020 nas fontes de dados: MEDLINE (via PubMed), EMBASE, Scopus e Literatura Latino-Americana e do Caribe em Ciências da Saúde, National Guideline Clearinghouse e Guidelines International Network, e sites do Ministério da Saúde do Brasil, Sociedades Médicas Brasileiras, Conselhos de Medicina, Conselho Federal de Enfermagem e Conselho Federal de Fisioterapia. A avaliação da qualidade metodológica e da transparência das diretrizes ocorreu por meio do instrumento Appraisal of Guidelines for Research & Evaluation, versão II, realizada por quatro autores. Resultados: Foram encontradas 33 diretrizes, das quais foram incluídas 14 para análise. Somente uma diretriz apresentou pontuações acima de 60% em todos os domínios. Entre os seis domínios, três apresentaram maiores pontuações: Escopo e finalidade, Envolvimento das partes interessadas e Clareza da apresentação. Discussão: Apesar da fragilidade metodológica, os autores se preocuparam em apresentar as recomendações de forma clara e concisa, através de informações-chave e opções terapêuticas que facilitam a tomada de decisão. Conclusão: As diretrizes brasileiras apresentaram baixa qualidade metodológica, em que somente uma diretriz foi recomendada e classificada com alta qualidade e transparência metodológica.
Palabras chave:Infecções por Coronavirus; Pandemias; Revisão Sistemática; Guias como Assunto; Terapêutica.
Abstract
Introduction: Coronavirus disease (Covid-19) is an infectious disease affecting the respiratory tract, which emerged in China and spread rapidly throughout the world. Objective: To evaluate the methodological quality and transparency of Brazilian clinical practice guidelines for the treatment of coronavirus disease (Covid-19). Materials and Methods: A systematic review was conducted in 2020 on Medline (via PubMed), Embase, Scopus, LILACS, National Guideline Clearinghouse and Guidelines International Network databases, in addition to online searches on the Brazilian Ministry of Health, Brazilian Medical Association, Federal Council of Medicine, Federal Council of Nursing and Federal Council of Physical Therapy websites. The methodological quality and transparency of the guidelines were assessed using the second version of the Appraisal of Guidelines for Research and Evaluation (AGREE) instrument developed by four authors. Results: 33 guidelines were found of which 14 were included in the analysis. There was only one guideline that scored above 60% in all domains. Among the six domains, higher scores were found in the following three domains: scope and objective, stakeholder involvement and clarity of presentation. Discussion: Despite methodological weakness found, the authors were keen to provide clear and concise recommendations through key information and therapeutic options to facilitate decision making. Conclusions: Brazilian clinical practice guidelines were found to be of poor methodological quality, from which only one guideline was recommended and classified as to be of high methodological quality and transparency.
Keywords: Coronavirus Infections; Pandemics; Systematic Review; Guidelines as Topic; Therapeutics
Resumen
Introducción: La enfermedad por coronavirus (Covid-19) es una patología infecciosa que afecta al sistema respiratorio, la cual se originó en China y se extendió rápidamente por todo el mundo. Objetivo: Evaluar la calidad metodológica y la transparencia de las guías de práctica clínica brasileñas para el tratamiento de la enfermedad por coronavirus (Covid-19). Materiales y métodos: Se realizó una revisión sistemática en 2020 en las bases de datos Medline (vía PubMed), Embase, Scopus, LILACS, National Guideline Clearinghouse y Guidelines International Network, además de consultas en los sitios web del Ministerio de Salud de Brasil, Asociación Médicas Brasileña, Consejo Federal de Medicina, Consejo Federal de Enfermería y Consejo Federal de Fisioterapia. La evaluación de la calidad metodológica y la transparencia de las guías se realizó con el instrumento Appraisal of Guidelines for Research and Evaluation (AGREE), segunda versión realizada por cuatro autores. Resultados: Se encontraron 33 guías, de las que se incluyeron 14 en el análisis. Hubo una sola guía que obtuvo una puntuación superior al 60% en todos los dominios. Entre los seis dominios, se presentaron puntuaciones más altas en los siguientes tres dominios: alcance y objetivo, participación de las partes interesadas y claridad de la presentación. Discusión: A pesar de la fragilidad metodológica, los autores se interesaron por presentar las recomendaciones de forma clara y concisa a través de información clave y opciones terapéuticas que faciliten la toma de decisiones. Conclusión: Las guías de práctica clínica brasileñas mostraron tener una baja calidad metodológica, de las que solamente una guía fue recomendada y clasificada como de alta calidad y transparencia metodológica.
Palabras clave: Infecciones por Coronavirus; Pandemias; Revisión Sistemática; Guías como Asunto; Terapéutica.
Introdução
A Coronavirus Disease-2019 (Covid-19) é uma doença infectocontagiosa provocada pelo coronavírus-2 (SARS-CoV-2) que afeta o sistema respiratório, causando sintomas como dispneia, febre, fadiga muscular, dor, náuseas, vômitos, diarreia, entre outros, além de casos clínicos assintomáticos1. Inicialmente, a doença foi detectada na China com investigação da etiologia de casos clínicos de pneumonia e síndrome respiratória aguda grave, e logo se disseminou rapidamente pelo mundo, causando elevadas taxas de contágio e mortalidade2.
Atualmente, nenhum tratamento específico para a Covid-19 foi encontrado, mas alguns medicamentos e manejos clínicos são usados para auxiliar no tratamento da infecção associada a doenças respiratórias leves a graves, com intuito de reduzir os sinais clínicos e fornecer cuidados de suporte1,3. Vários fármacos estão sendo testados, além da adoção de medidas de precaução e suporte ventilatório em pacientes graves, os quais são discutidos por especialistas na área, e as evidências que surgem são utilizadas para elaboração de diretrizes com intuito de orientar os profissionais de saúde sobre a doença4.
O fornecimento da assistência de suporte é fundamental para a recuperação dos pacientes. Para tal, é necessário investimento em documentos que abarquem diagnóstico e tratamento mais apropriados, sendo embasados em evidências desenvolvidas por meio de métodos clínicos e testados por especialistas. Estes documentos são diretrizes clínicas que devem estar disponíveis e de fácil compreensão e acesso tanto aos profissionais de saúde, quanto à comunidade, sendo fundamentais para auxiliar na tomada de decisão4.
As Diretrizes de Prática Clínica (CPGs) são definidas como o conjunto de informações desenvolvidas sistematicamente por profissionais referenciados de conselhos e associações de saúde, com base em evidências científicas, para assistir nas decisões acerca de cuidados apropriados para cada circunstância clínica do paciente4-5. Contudo, para que uma diretriz possa servir como recomendação e também ser útil para a prática clínica, faz-se necessário ter boa relevância científica e uma elevada complexidade metodológica para referenciá-la6-7.
Alguns métodos rigorosos são utilizados para avaliação das diretrizes clínicas, como a ferramenta Appraisal of Guidelines for Research & Evaluation, versão II (AGREE II), que é amplamente empregada para avaliar os procedimentos de desenvolvimento, sendo considerada "padrão ouro" para a análise metodológica das CPGs8. Destaca-se que o rigor metodológico do processo de desenvolvimento de diretrizes é importante para a implementação adequada das recomendações e assegurar sua aplicabilidade em contextos de saúde com alcance de usuários e profissionais da área8.
Em fevereiro e março de 2020, com o primeiro caso confirmado e óbito registrado de Covid-19 no Brasil, despertou a preocupação em desenvolver protocolos de diagnóstico e tratamento da doença9. Na literatura foi encontrada somente uma revisão sobre avaliação metodológica de diretrizes4, entretanto, nenhuma com enfoque em documentos brasileiros.
Dessa forma, objetivou-se avaliar a qualidade metodológica e transparência das CPGs brasileiras para o tratamento da Covid-19. Delineou-se como questão de revisão: "Qual a qualidade metodológica e transparência das CPGs brasileiras para o tratamento da Covid-19?".
Materiais e Métodos
Revisão sistemática de avaliação da qualidade metodológica e transparência das CPGs brasileiras para o tratamento da Covid-19, por meio do instrumento AGREE II. Esta revisão sistemática foi registrada no PROSPERO (CRD42020180876) e seguiu as recomendações do PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses), um guia que descreve as exigências específicas para estudos de revisões sistemáticas e metanálises10. Foram incluídas as CPGs brasileiras que contemplam as recomendações de tratamento da Covid-19 para crianças, adultos e idosos, escritas em português, inglês ou espanhol, publicadas até junho de 2020. As CPGs brasileiras com texto completo indisponível ou com apenas o resumo das recomendações disponível foi excluído.
A pesquisa bibliográfica foi realizada na MEDLINE (via PubMed), EMBASE, Scopus e LILACS, utilizando as combinações de palavras-chave, descritores e MeSH, conforme: covid-19; pneumonia, viral; infecção do coronavírus; pandemia, nova doença coronavírus 2019, infecção SARS-CoV-2, doença por vírus covid-19, infecção 2019-nCoV, doença do coronavirus 2019, coronavirus, doença-19, doença 2019-nCoV, 2019-nCoV, infecção pelo vírus Covid-19, vírus Covid-19, diretrizes práticas, melhor prática, guias de prática clínica, diretivas práticas, diretivas de prática clínica, diretivas de prática médica, diretivas para a prática clínica, diretivas para a prática médica, diretrizes diagnósticas, diretrizes práticas, diretrizes de prática médica, diretrizes para a prática clínica, diretrizes para a prática médica, guias de prática médica e guias para a prática médica.
Para a combinação dos termos foram utilizados os operadores booleanos AND e OR, e os termos foram usados nos idiomas inglês, português e espanhol (as combinações das estratégias estão no material suplementar). Além disso, foram acessados os documentos disponíveis em bases de dados internacionais de CPGs, como National Guideline Clearinghouse (NGC) e Guidelines International Network (GIN). Também foram realizadas buscas na literatura cinzenta, especialmente nos sites do Ministério da Saúde do Brasil, Sociedades Médicas Brasileiras, Conselhos de Medicina, Conselho Federal de Enfermagem e Conselho Federal de Fisioterapia.
A seleção das CPGs foi realizada entre maio e junho de 2020 por dois revisores (revisor A e B) que avaliaram de forma duplo-independente os títulos e resumos para potencial elegibilidade. Os revisores realizaram a análise de cada artigo em texto completo de acordo com os critérios de seleção. As publicações indexadas em mais de uma base de dados foram incluídas apenas uma vez, restando, portanto, 33 diretrizes para análise, conforme a Figura 1.
Figura 1. Fluxograma Prisma do processo de seleção das CPGs brasileiras
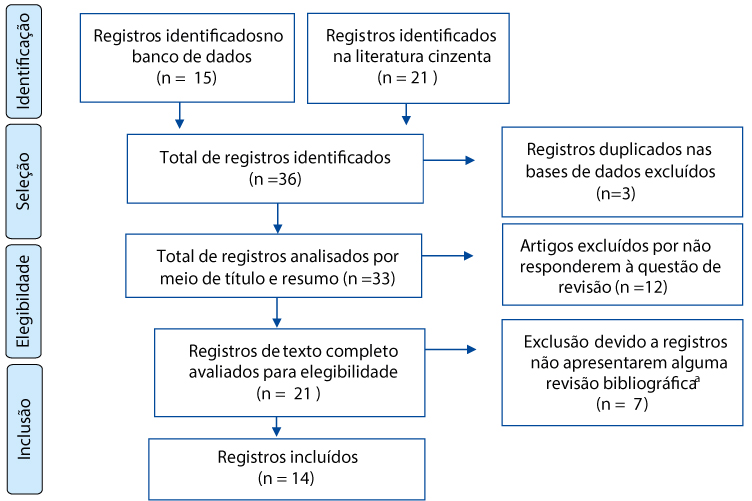
aquaisquer diretrizes devem ser realizadas com base em evidências científicas.
O revisor A incluiu oito diretrizes e o revisor B, 13. Diante da divergência de seleção, os cinco artigos excluídos pelo revisor A e um artigo excluído pelo revisor B foram reavaliados e incluídos através do consenso entre os dois revisores, totalizando 14 CPGs brasileiras incluídas nesta revisão.
A extração dos dados das 14 CPGs foi realizada pelo revisor A, por meio de uma planilha do Microsoft Excel desenvolvida para esta pesquisa. O revisor B verificou as informações coletadas pelo revisor A, analisando a relevância dos dados extraídos, não havendo nenhuma discrepância nas informações. As CPGs foram avaliadas quanto à população-alvo, presença de uma revisão sistemática (sim ou não), presença de métodos de classificação de evidências (sim ou não), qualidade de avaliação e tipos de recomendações (diagnóstico, profilaxia, tratamentos farmacológicos e manejo clínico).
A avaliação da qualidade metodológica e da transparência das CPGs ocorreu por meio do instrumento AGREE II11. O AGREE II é composto por 26 itens divididos por seis domínios: Escopo e finalidade; Envolvimento das partes interessadas; Rigor do desenvolvimento; Clareza da apresentação; Aplicabilidade; e Independência editorial11-13. Os revisores foram treinados para manusear o instrumento AGREE II de acordo com a ferramenta de treinamento online e um teste piloto com avaliação de duas CPGs para verificar a compreensão adequada do instrumento. A avaliação das CPGs brasileiras ocorreu de forma individual e independente por quatro revisores, formados por: revisor A e B da etapa de seleção e extração dos dados, e por dois revisores C e D, incluídos para esta etapa. As discrepâncias foram resolvidas por consenso entre os revisores11-13.
O grau de concordância entre os quatro revisores (A, B, C e D) foi calculado com base no coeficiente de correlação intraclasse: ˂ 0,4 = ruim; 0,4 ≤ a ˂ 0,75 = satisfatório e ≥ 0,75 = excelente14. Os dados descritivos das CPGs incluídas e os tipos de recomendações foram extraídos acerca de diversos aspectos categorizados, com seus respectivos índices de qualidade metodológica, calculados por meio do AGREE II.
O instrumento AGREE II não apresenta valores limites para a classificação da qualidade metodológica das diretrizes, entretanto, recomenda que os autores definam os limites individuais apropriados para a sua revisão. Para esta revisão, foram considerados valores limítrofes de acordo com publicações anteriores, sendo definido escore suficiente de qualidade acima de 60%, e uma diretriz foi considerada recomendável se a maioria dos domínios (quatro ou mais) ultrapassasse esse limite15-16. Caso as diretrizes apresentassem valores inferiores a 60% em quatro ou mais domínios, seria classificada como de baixa qualidade, não sendo recomendada15-16.
Resultados
Foram incluídas 14 CPGs acerca da Covid-19 desenvolvidas para pacientes suspeitos e diagnosticados com coronavírus (57,1%; n = 8)17-24 em serviços de atenção à saúde hospitalar e não hospitalar (57,1%; n = 8)17,19-20,25-29, sendo o manejo clínico de pacientes com Covid-19 a principal recomendação aos profissionais de saúde (42,9%; n = 6)21-24,29-30, conforme a Tabela 1.
Tabela 1. Caraterísticas das CPGs brasileiras acerca da Covid-19
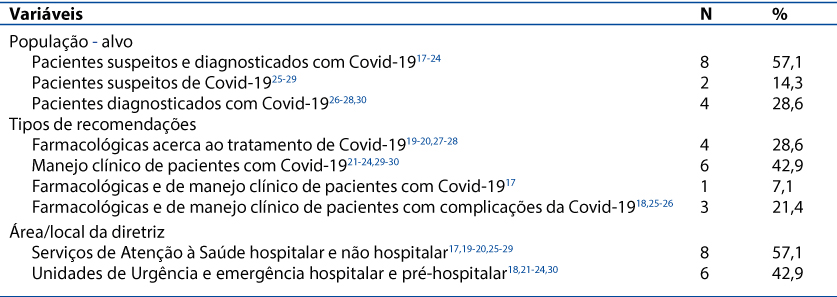
As principais recomendações de manejo clínico foram sobre os cuidados e tratamentos mais adequados de oxigenoterapia21-24,29-30, com destaque para a necessidade de os profissionais de saúde realizarem o manejo correto e seguro durante os procedimentos. Já, referente às recomendações farmacológicas utilizadas no tratamento da Covid-19, se destacaram: lopinavir/ritonavir (21,4%; n = 3)19-20,27, sulfato de hidroxicloroquina (21,4%; n = 3)19-20,27 e difosfato de cloroquina (14,3%; n = 2)20,27, antibioticoterapia (14,3%; n = 2)19,29, corticosteroides (14,3%; n = 2)19,27, tocilizumabe (14,3%; n = 2)19,27, oseltamivir (14,3%; n = 2)27-28 e heparina (14,3%; n = 2)27-28.
No que se refere às informações utilizadas na construção das CPGs, percebeu-se que somente 14,3% (n = 2)19,28 utilizaram resultados de revisões sistemáticas como fontes de evidências para o desenvolvimento das recomendações, as quais foram classificadas por meio da ferramenta Grade. As demais CPGs utilizaram as evidências da literatura sem mencionar a avaliação crítica, consulta a especialistas na área, experiências e lições aprendidas de outros países (85,7%; n = 12)17-25,27,29-30.
Na Tabela 2, são apresentados os escores do AGREE II das CPGs incluídas nesta revisão.
Tabela 2. Escores dos seis domínios do AGREE II das CPGs brasileiras da Covid-19
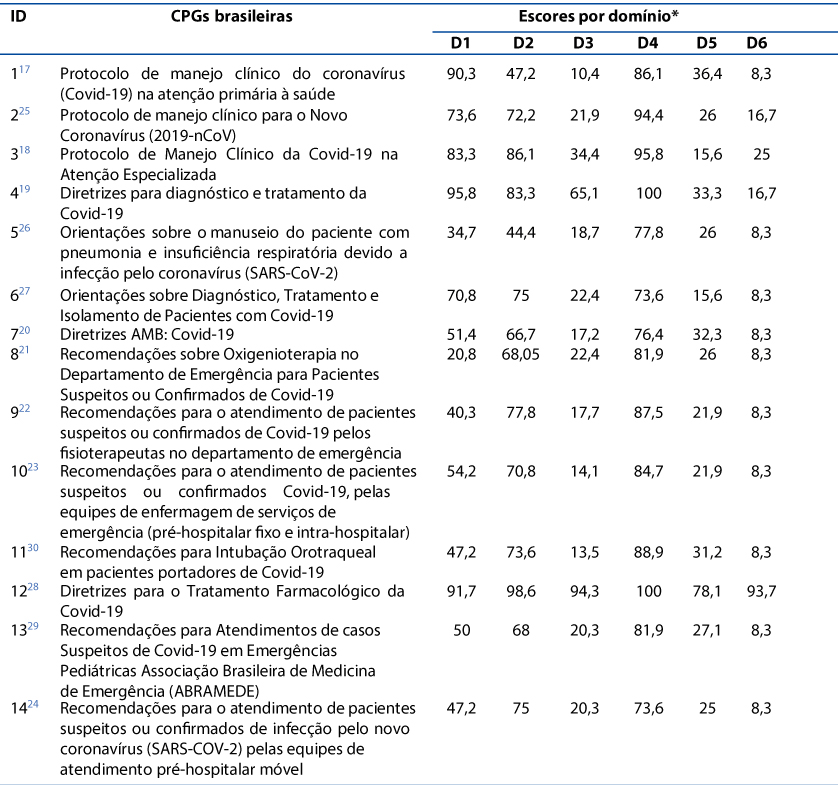
Legenda = CPGs: Diretrizes de Prática Clínica; ID: código de identificação das diretrizes; D1: Domínio Escopo e finalidade; D2: Dominio Envolvimento das partes interessadas; D3: Domínio Rigor do desenvolvimento; D4: Domínio Clareza da apresentação; D5: Domínio Aplicabilidade; D6: Domínio Independência editorial. *valores em porcentagem (%).
Conforme a Tabela 2, nove17,20-24,26,29-30 das 14 CPGs tiveram pontuações inferiores a 60% em quatro ou mais domínios, sendo classificadas com baixa qualidade, não sendo recomendadas pelos avaliadores. Somente a diretriz ID1228 apresentou pontuações acima de 60% em todos os domínios, variando entre 78,1% e 100%, sendo a única CPG recomendada por todos os avaliadores e classificada com alta qualidade e transparência metodológica, sem necessidade de modificações. Somente quatro18-19,25,27 CPGs foram recomendadas com modificações pelos avaliadores.
Dentre os seis domínios, se destacaram "Rigor do desenvolvimento", "Aplicabilidade" e "Independência editorial" com pontuações mais inferiores, e os domínios "Escopo e finalidade", "Envolvimento das partes interessadas" e "Clareza da apresentação" receberam as maiores pontuações.
Na Tabela 3, está apresentada a confiabilidade da concordância entre os avaliadores na classificação das CGPs por meio do AGREE II
Tabela 3. Confiabilidade da concordância entre os avaliadores na avaliação das CPGs brasileiras, conforme o AGREE II
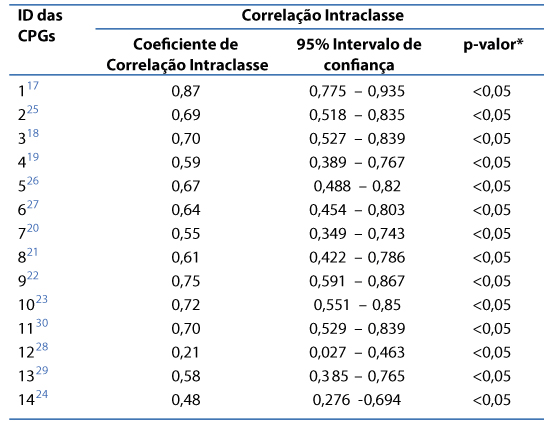
ID: código de identificação das Diretrizes de Prática Clínica brasileiras; * valores significativos para < 0,05
O coeficiente de correlação intraclasse variou entre os protocolos de 0,21 a 0,87 (ID 1228 e ID 117, classificados como pobre e satisfatório, respectivamente), em que 92,8% das CPGs17-27,29-30 tiveram um grau satisfatório a excelente de concordância na classificação da qualidade metodológica entre os avaliadores.
Discussão
Este estudo traz importantes resultados sobre a elaboração de protocolos clínicos em tempos de pandemia para o tratamento da Covid-19. As CPGs são fundamentais para guiar os profissionais de saúde para a tomada de decisão, e a avaliação dessas diretrizes se faz necessária para determinar a qualidade e transparência metodológica para o tratamento da Covid-1911,31.
Para a avaliação das diretrizes foi selecionada uma equipe multidisciplinar e interdisciplinar, como orientado pelo instrumento AGREE II, e utilizada em outros estudos, a fim de alcançar uma avaliação eficiente e abrangente32. Em busca realizada nas fontes de dados, as diretrizes brasileiras publicadas e selecionadas para este estudo são utilizadas para os serviços de atenção à saúde hospitalar e não hospitalar17,19-20,25-29 e contêm as principais recomendações aos profissionais de saúde para os cuidados e tratamentos destinados aos pacientes.
Quanto às recomendações, prevaleceu o manejo clínico dos pacientes com Covid-1921-24,29-30 com destaque para a oxigenoterapia21-24,29-30, a qual é um dos tratamentos essenciais para pacientes clinicamente graves com a síndrome do desconforto respiratório agudo, complicação causada pelo coronavírus33. As recomendações farmacológicas utilizadas no tratamento da Covid-19 foram as terapias antivirais, as quais estão sendo analisadas e testadas19-20,27, entretanto, ainda com resultados clínicos de pouca consistência34, demandando maior investimento em pesquisas de caráter de ensaio clínico duplo-cego randomizado33.
Os resultados de pesquisas de ensaios clínicos são considerados "padrão ouro" na elaboração das recomendações, os quais fornecem fortes evidências para a prática e atenção integral à saúde dos pacientes. Fornecem dados suscetíveis a menores riscos de vieses na investigação da relação de causa e efeito sobre os resultados de determinada intervenção de manejo clínico ou farmacológico no tratamento da doença35-36.
Diante dos resultados apresentados, de modo geral, as diretrizes carecem de evidências com adequada qualidade metodológica, o que impossibilita recomendações mais categóricas31. A utilização de metodologias apropriadas e estratégias rigorosas em seu processo de desenvolvimento faz com que a qualidade das diretrizes seja melhor, conferindo confiabilidade ao seu uso para a prática clínica12-13.
Dessa forma, somente uma diretriz foi recomendada e classificada com alta qualidade e transparência metodológica, e quatro recomendadas com algumas modificações, enquanto nove tiveram pontuações inferiores a 60% em quatro ou mais domínios. A baixa qualidade e transparência metodológica das CPGs brasileiras é justificada pelos objetivos das diretrizes, as quais refletem os tratamentos farmacológicos e manejos clínicos de pacientes diagnosticados com a Covid-19 que ainda não apresentam tratamentos efetivamente comprovados. Além disso, muitas diretrizes foram elaboradas no início da pandemia, momento de maior criticidade devido ao acelerado aumento de pessoas infectadas, tendo a necessidade de estudos clínicos e de diretrizes que abarcassem tratamentos mais efetivos para atender a população37-38.
Dentre os domínios o "Rigor do desenvolvimento" (D3), "Aplicabilidade" (D5) e "Independência editorial" (D6) tiveram pontuações mais inferiores. Os domínios D3 e D6 são considerados como os de maior influência na qualidade geral de uma diretriz, por se referirem ao padrão metodológico com que uma CPG deve ser construída. É importante que o desenvolvimento de diretriz siga um rigor na metodologia para que seja aplicada em diversos serviços, especialmente na área da saúde, com a declaração de quaisquer tipos de influência e/ou conflitos entre as organizações financiadoras e o conteúdo do documento39. Ressalta-se que raramente as instituições financeiras fazem declaração explícita de que seus interesses não influenciaram as recomendações, entretanto, são cruciais para uma boa avaliação40-41.
Estes achados estão de acordo com três estudos anteriores42-44, e podem ser justificados pelo motivo de que, nos primeiros meses de pandemia, diante da falta de evidências científicas, tinha-se a necessidade emergente de informações para embasar o tratamento dos pacientes diagnosticados com a Covid-1943. Além disso, algumas diretrizes foram publicadas somente em sites de sociedades e organizações de saúde, sendo relatadas com poucas informações, resultando em baixa qualidade metodológica. Diante disso, é importante que os profissionais de saúde que utilizam as diretrizes na saúde pública e privada tenham o conhecimento de avaliação da qualidade, para melhor orientar sua prática assistencial, assim como considerar as evidências embasadas em estudos clínicos43.
A baixa pontuação do domínio D5 se deve à falta de descrição das potencialidades, riscos, benefícios e estratégias na implementação das recomendações, as quais, na maioria, se referem ao uso farmacológico no tratamento da Covid-19, em que ainda persistem dúvidas e que necessitam de maior investigação40.
Os domínios "Escopo e finalidade" (D1), "Envolvimento das partes interessadas" (D2) e "Clareza da apresentação" (D4) receberam as maiores pontuações, conforme os achados da literatura40-41. Estes domínios se referem à apresentação da finalidade e à população a quem são destinadas as recomendações, descrevendo as partes interessadas como os grupos profissionais e usuários das recomendações11-13. Percebe-se que os autores se preocuparam em deixar claros a finalidade dos tratamentos, o envolvimento dos usuários, as condições e problemas de saúde, por se tratar de uma doença com nenhuma intervenção terapêutica estabelecida. Esta preocupação reflete na apresentação adequada das recomendações e na sua finalidade, através de informações-chave e opções terapêuticas que facilitam a tomada de decisão clínica41.
No que concerne à concordância entre os avaliadores das diretrizes, 92,8% das CPGs brasileiras tiveram um grau satisfatório a excelente de concordância na classificação da qualidade metodológica, evidenciando mínima variação interobservador e grau adequado de concordância na avaliação das diretrizes14,45.
No contexto atual, a falta de rigor metodológico nas CPGs brasileiras requer incentivos para o seu desenvolvimento com base em evidências científicas de revisões de alta qualidade, com o propósito de alcançar recomendações consistentes para auxiliar a assistência. As instituições responsáveis pela elaboração das CPGs necessitam fortalecer a colaboração de especialistas multidisciplinares, com o intuito de reduzir o risco de viés na atualização e elaboração de novos guias, assim como melhorar aplicabilidade das recomendações40.
Como lacuna, ressalta-se que, apesar de o AGREE II ser aplicável para avaliação de guias clínicos, a ferramenta foi destinada para diretrizes desenvolvidas por especialistas em condições não emergentes, como não é o caso da pandemia da Covid-19, o que pode ter influenciado nos resultados deste estudo. Ademais, é estimado que algumas diretrizes elaboradas no início da pandemia e incluídas nesta revisão foram atualizadas, e outras desenvolvidas após este estudo. Finalmente, esta pesquisa pode servir como base para estudos futuros para avaliar as mudanças na atualização e elaboração de novas CPGs no decorrer da pandemia.
Conclusão
As CPGs brasileiras acerca da Covid-19 apresentaram baixa qualidade metodológica, conforme a avaliação do AGREII, em que somente uma diretriz foi recomendada e classificada com alta qualidade e transparência metodológica. Dentre os seis domínios, somente três apresentaram maiores pontuações: Escopo e finalidade, Envolvimento das partes interessadas e Clareza da apresentação.
No que concerne à concordância de avaliação das CPGs, evidenciou-se grau satisfatório a excelente entre os quatro avaliadores, sendo verificado a partir do cálculo de correlação de intraclasse. Portanto, reforça-se a importância da elaboração e reformulação das CPGs da Covid-19 no sentido de adequar o rigor metodológico, descrevendo de forma mais clara e concisa sobre a aplicabilidade das recomendações e esclarecendo a independência editorial e a existência de conflito de interesses.
Conflitos de Interesse: Os autores declaram que não há conflitos de interesse.
Financiacion: Os autores declaram que não há fontes de financiamento.
Referências